In China for Global | 美国篇
纽约还行加州也凑合
一不留神新泽西~
全球医药消费市场中,美国市场份额占38.7%,由于强大的市场份额和绝对的支付能力,多数药企选择美国作为“出海”首站。随着FDA审核制度日益趋严,国产创新药出海难度不断攀升,据《中国商界》统计2021年我国有8款创新药的新药申请/生物制品许可申请获FDA受理,但仅有传奇生物旗下1款产品成功获批;今年我国多家头部企业折戟FDA审批,虽付出了惨痛的代价,但也为后续闯关美国提供了宝贵的经验。
临床“出海”美国需要注意哪些事项?管理制度、政策法规和国内有何差异?杉互君今天就给大家带来"In China for Global"系列第3篇——美国篇。
中心类型差异
美国医疗系统庞大且复杂,不同规模医疗机构遍布各州,且医院分类无严格定义及标准。与我国不同,美国临床试验研究中心无需美国FDA或其他部门认证,且对医院性质、级别无特殊限定要求。研究中心包括大型学术教学医院、社区医院、私人诊所、独立研究中心、临床试验现场管理组织(SMO) /临床试验联合体5大类,不同类型研究中心都各有特点。其中大型学术教学医院代表着美国医院和医学领域最先进水平,不仅为患者提供疑难杂症诊疗,更担负着前沿领域科教工作。美国研究者信息化系统操作经验丰富,但部分研究中心有严格网关限制,国内登录服务器并不友好,如何解决跨国网络限制?别担心,杉互在美国部署专用服务器,各项目独立分配专属URL,可实现全球范围秒级交互。

图:美国临床试验研究中心主要类型和特点
数据采集标准
听说XX供应商被FDA认证了?认证?不存在的!FDA数据采集标准 21 CFR Part 11 才是整个行业的指导原则。作为美国1997年8月颁布实施的一项FDA法规,其规范了FDA监管工作中电子记录、电子签名的标准。可信和可靠是电子记录及电子签名的基本准则,也是行业要求的体现,满足规范的电子记录与书面记录效力同等,电子签名可等同手写签名。特别需要关注的是 21 CFR Part 11 作为FDA监管工作中基本准则,对全球整个行业的数据采集标准具有深度的影响力。
那么有关信息化系统,美国监管部门会重点关注哪些方面呢?杉互君总结多项海外案例实操经验,发现“权限管理”、“盲态保护”、“随机重现”三大重点需格外关注。
药物警戒人员非盲权限如何设置?
FDA允许PV揭盲么?
非盲人员更迭后,需要多久失活账户?
未及时处理的账户,会成为major finding?
研究中心要求更换非盲护士为盲态护士怎么办?
紧急揭盲需要medical scientist批准么?
二次随机FDA如何要求?
随机可以百分之百重现么?
SAS&种子 VS 系统程序&种子有什么区别?
不要慌,这些问题我们都经验满满。杉互健康以系统强大算法为基础配合丰富既往国际研究经验,赋能临研团队、加速研究启动,助力50+国际研究成功落地。
审批流程差异
美国除大型学术医院组织架构和审批管理流程较全面,其他类型临床研究中心设置和职能较为单一。美国的审批内容与我国基本相似,但由于体制背景等因素,具体执行存在一定区别。在美国递交研究项目时,需先经同领域专家进行同行审评,对研究项目的科学性、可行性、研究团队资质等进行评估;后经科学审评委员审评,对研究方案的科学性及合理性、立题依据的充分性、风险控制措施等提出建议与意见。那么针对系统,研究中心会如何考核供应商资格?数据修改流程中美之间有何差异?跨时区支持,培训有哪些注意点?紧急情况下,国内供应商的解决方案如何?这些问题杉互都很在行!
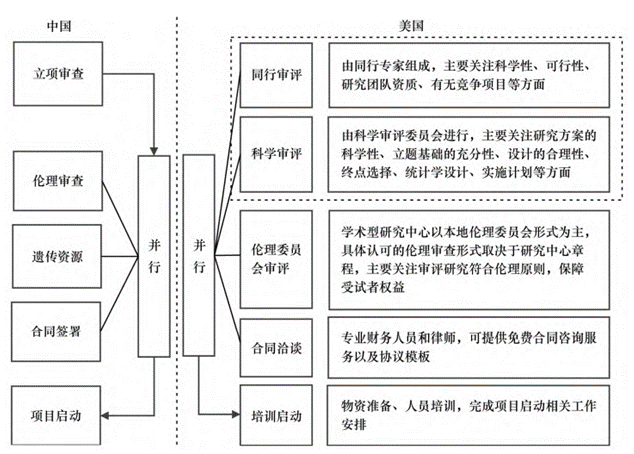
图:中美学术型机构临床试验审评阶段的类比分析
近年来在国家政策支持、企业研发深入、机构积极响应等多方面努力下,中国药企在国际舞台上发出越来越响亮的声音。杉互君也希望能在国产创新药“出海”远航中助力更多企业披荆斩棘、乘风破浪!
In China for Global,下一期杉互君将带领大家“出海”何方,敬请期待~
联系我们
电话:15921007226
邮箱:bd@irtone.com
热线:400-1616-835
参考资料:
[1]房虹,汤骐羽,何静,沈晔,樊琦,黄慧瑶,吴大维,孙超,王书航,陶魏,方元,李宁,唐玉.中美临床研究中心管理模式及启动效率的对比分析[J].中国新药杂志,2022,31(12):1195-1200.
[2]智会静,冯红云,周凌芸,杨建红,吕心欢,黎泽琳,李浩.新药临床试验期间药物警戒和风险控制研究一:欧美新药临床试验期间药物警戒体系要求对我国申办者的启示[J].中国药事,2022,36(06):618-623.DOI:10.16153/j.1002-7777.2022.06.003.
[3]https://www.zhihu.com/zvideo/1446886249206710272.

